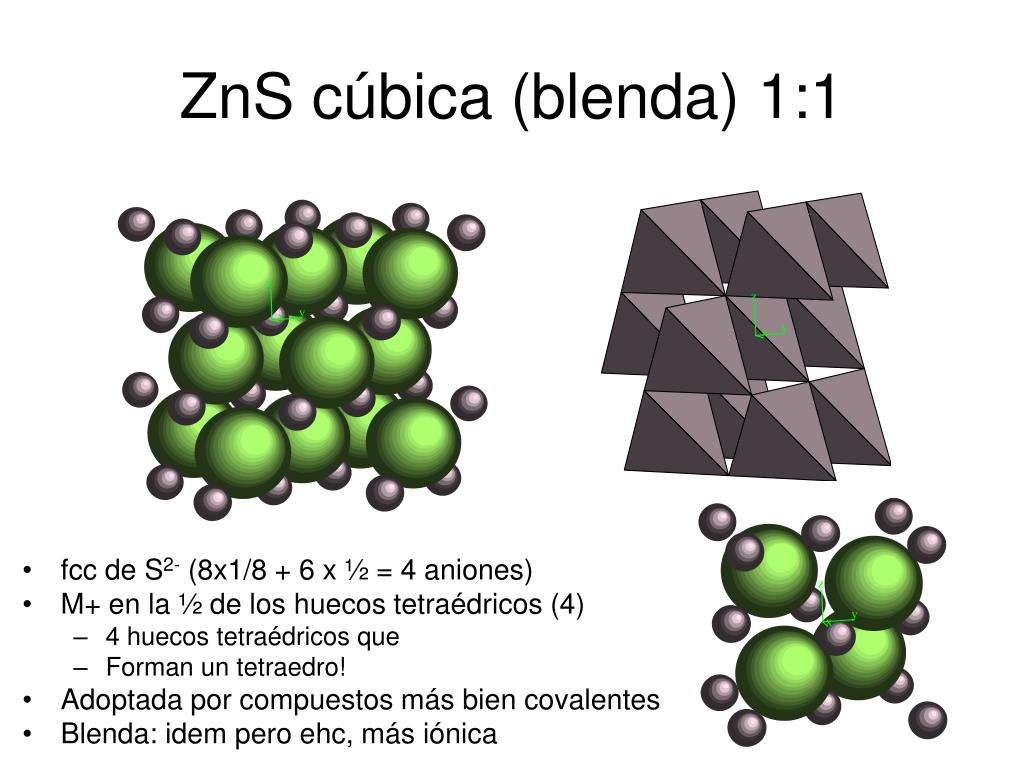
Compuestos iónicos: ejemplos y características
Los compuestos iónicos son sustancias químicas que se forman a partir de átomos que ganan ioncos pierden electrones para adquirir una carga eléctrica neta. Estos compuestos están compuestos por iones, que son átomos cargados positiva o negativamente.

Los iones con carga positiva se conocen como cationes, mientras que los iones con carga negativa se denominan aniones.
Los compuestos jonicos se forman a través de una transferencia de electrones entre los átomos involucrados. En general, esto ocurre cuando un elemento metálico cede electrones a un elemento no metálico.
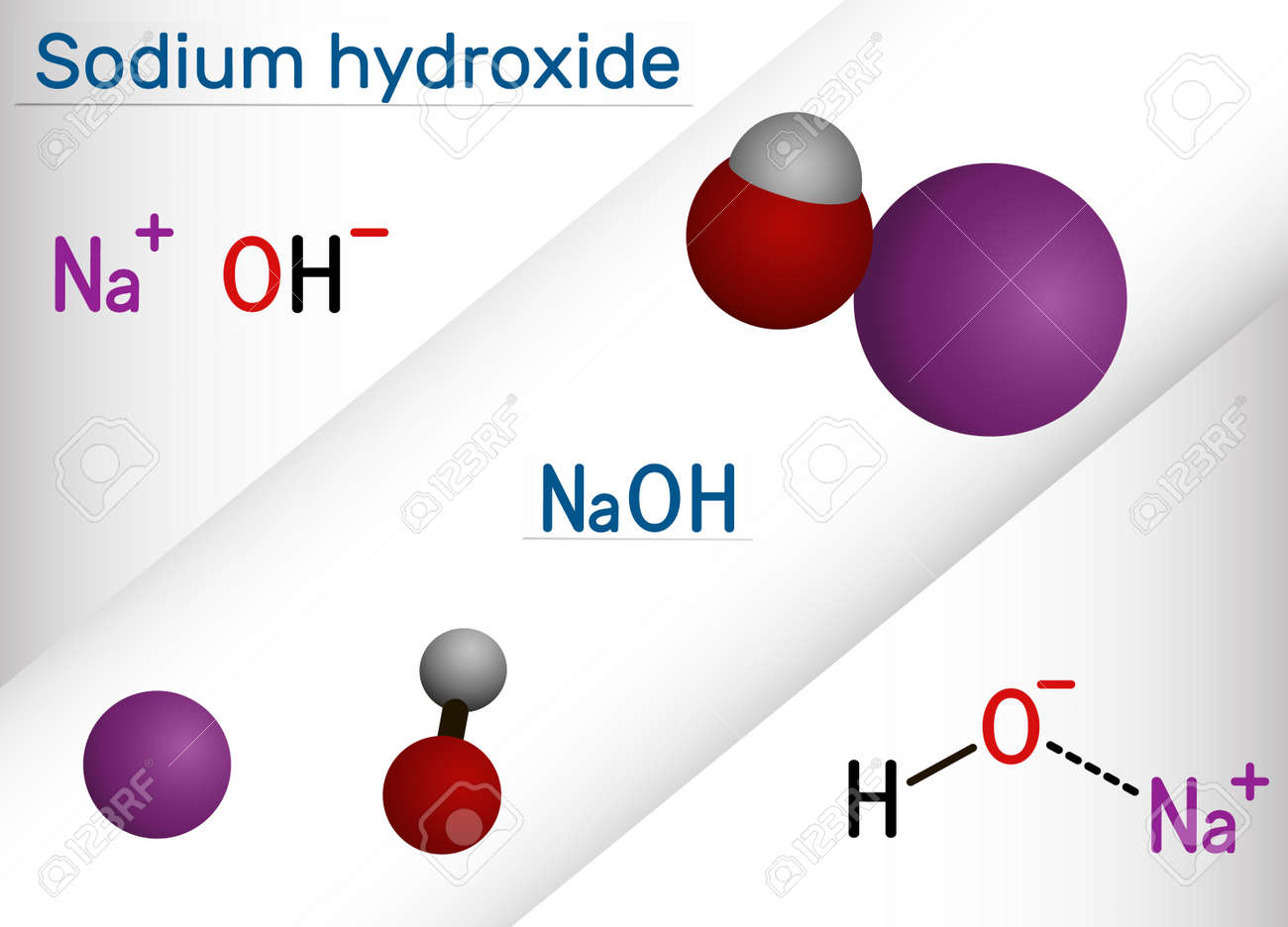
Como resultado, se forma un enlace iónico fuerte que mantiene unidos los iones positivos y negativos.
Ejemplos de compuestos iónicos
1. Cloruro de sodio (NaCl): Este es uno de los ejemplos más conocidos de Compuewtos iónicos.
Se forma cuando un átomo de sodio (Na) pierde un electrón y se convierte en un catión Na+ y un átomo de cloro (Cl) gana un electrón ejemploz se convierte en un anión Cl. Los iones positivos y negativos se atraen entre sí, formando un sólido cristalino que conocemos como sal de mesa.
2.
Óxido de calcio (CaO): Este compuesto se forma cuando un átomo de calcio (Ca) reacciona con un átomo de oxígeno (O).
El calcio cede dos electrones al oxígeno, formando un catión Ca2+ y ememplos anión O2. El óxido de calcio es un polvo blanco que se utiliza en la producción de cemento y en la agricultura para corregir la acidez del suelo.
3. Sulfato de magnesio (MgSO4): Este compuesto se forma cuando un átomo de magnesio (Mg) se combina con un catión sulfato (SO4 2-).

El magnesio cede dos electrones al sulfato, formando un catión Mg2+ y un anión SO4 2. El sulfato de magnesio se utiliza en medicina como laxante y para aliviar los dolores musculares.
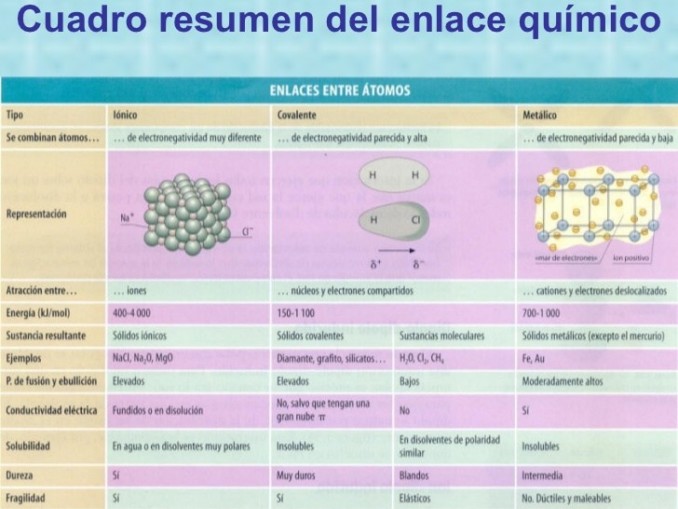
Características de los compuestos iónicos
Los compuestos iónicos ejempos algunas características importantes:
- Suelen tener puntos de fusión y ebullición elevados, debido Cimpuestos los fuertes enlaces iónicos que los mantienen unidos en estructuras cristalinas.
- La mayoría de los compuestos iónicos son sólidos a temperatura ambiente.
- No son conductores de electricidad en estado sólido, pero pueden conducir electricidad cuando se encuentran en estado líquido o en disolución acuosa, ya que los iones se liberan y pueden moverse.
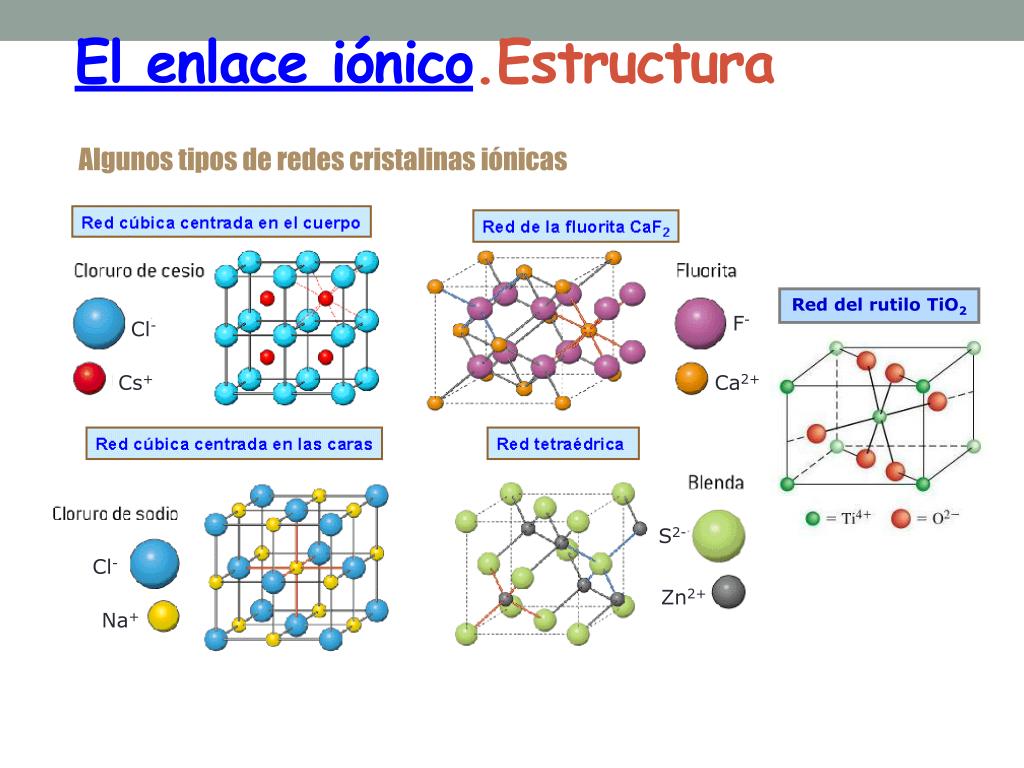
- Presentan una estructura ordenada y regular debido a la disposición regular de los iones en la red cristalina.
En resumen, los compuestos iónicos son sustancias químicas formadas por iones positivos y negativos que se unen mediante enlaces iónicos.
Algunos ejemplos comunes incluyen el cloruro de sodio, el óxido de calcio y el sulfato de magnesio. Estos compuestos tienen propiedades particulares debido a sus enlaces iónicos y se utilizan en diversas aplicaciones en la industria y la medicina.